Veelgestelde vragen over stamcellen
Kathrin Rothfischer studeerde microbiologie en genetica in Regensburg na een excursie naar Duitse studies. Complexe vraagstukken op een begrijpelijke manier presenteren was toen al haar passie. Daarom heeft ze na haar afstuderen van deze passie haar beroep gemaakt: Na verschillende functies bij de medisch specialistische uitgeverij en in de publieke pers vond ze eindelijk haar journalistieke thuis bij
Meer over de experts Alle inhoud van wordt gecontroleerd door medische journalisten.Stamcellen worden beschouwd als belangrijke dragers van hoop voor de therapie van verschillende ziekten. De meest voorkomende vragen over stamcellen
Wat zijn stamcellen?
De klassieke definitie van een stamcel is: zelfvernieuwing en meervoudig ontwikkelingspotentieel. Dit betekent dat stamcellen zichzelf kunnen vernieuwen en altijd nieuwe stamcellen kunnen produceren; ze zijn als het ware onsterfelijk. Elk ander type cel in het lichaam kan echter ook voortkomen uit een stamcel. Stamcellen zijn in principe een onuitputtelijke bron van vervangende cellen waarmee in theorie weefselschade kan worden hersteld.
Wat is het verschil tussen embryonale en volwassen stamcellen?
Volwassen stamcellen blijven in veel organen achter nadat het lichaam zich heeft ontwikkeld, bijvoorbeeld in de huid of in het bloed. Ze zijn ook zelfvernieuwend en hebben een regeneratief potentieel. Ze kunnen echter alleen cellen van een heel specifiek type weefsel vormen. Omdat ze voorgevormd zijn, zijn ze slechts in beperkte mate geschikt voor celvervangingstherapie. Embryonale stamcellen daarentegen zijn een volledig "blanco lei". In theorie kan elk type cel en dus elk type weefsel in het lichaam zich daaruit ontwikkelen.
Wat zijn pluripotente stamcellen?
Pluripotent houdt in dat een stamcel zich kan ontwikkelen tot alle celtypen van de drie kiemlagen van het embryo en daarmee tot alle cel- en weefseltypen in het lichaam. Het bekendste voorbeeld van een pluripotente stamcel is de embryonale stamcel. De laatste jaren zijn pluripotente stamcellen vooral bekend geworden als zogenaamde geïnduceerde pluripotente stamcellen.
Wat zijn geïnduceerde pluripotente stamcellen?
Wetenschappers zijn erin geslaagd om met behulp van bepaalde factoren normale lichaamscellen te verjongen en terug te brengen tot hun embryonale of stamcelstadium. Om dit te doen, smokkelden ze bepaalde controlegenen de lichaamscellen in. Uit de stamcellen die zo ontstaan, kweekten de onderzoekers verschillende soorten weefsel - zonder een embryo te vernietigen. Het risico: De kunstmatig gecreëerde pluripotentie kan het genetische materiaal van de cellen beschadigen. Tumoren en de ontwikkeling van kanker kunnen het gevolg zijn.
Waarom is er zo'n groot debat over stamcellen?
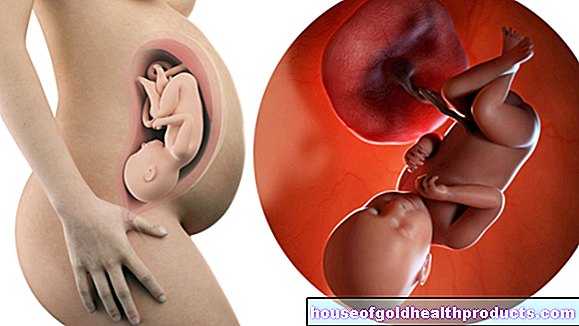
Embryonale stamcellen worden gevonden in de zogenaamde blastocyst, die ontstaat tussen de vierde en zevende dag na de bevruchting van een eicel. Om deze stamcellen te behouden, moet het embryo in een vroeg stadium worden vernietigd. Sommigen accepteren dit als een noodzakelijk kwaad, maar voor de critici betekent het het doden van levens. Wetenschappers hebben met behulp van geherprogrammeerde lichaamscellen een ethisch onschadelijk alternatief voor embryonale stamcellen gecreëerd. Deze methode is echter nog niet volledig ontwikkeld. Voor een effectieve therapie moeten eerst alle basismechanismen worden opgehelderd. Hiervoor is veel onderzoek nodig, op embryonale stamcellen. Omdat dit de gouden standaard is die moet worden begrepen.
Wanneer komt de eerste embryonale stamceltherapie?
Dat is moeilijk te zeggen. In oktober 2010 werd in de Verenigde Staten een gedeeltelijk verlamde man behandeld met embryonale stamcellen. Dit is de eerste officiële poging tot therapie met embryonale stamcellen bij mensen. Een jaar later werden de controversiële experimenten stopgezet wegens geldgebrek - zelfs als de celbereiding goed werd verdragen door de patiënten en er geen twijfelachtige bijwerkingen waren. Een ander onderzoek naar stamceltherapie voor leeftijdsgebonden maculaire degeneratie leverde de eerste positieve resultaten op. Maar dat is nog maar het begin. Om standaard een therapie aan te kunnen bieden zijn meerdere grote klinische onderzoeken nodig, die de veiligheid en effectiviteit van de behandeling aantonen. Dit is tijdrovend en kostbaar. Volgens experts kan het zelfs onder optimale onderzoeksomstandigheden tot 20 jaar duren voordat zieke mensen standaard kunnen worden behandeld met embryonale of geïnduceerde pluripotente stamcellen.
Welke ziekten kunnen in de toekomst worden genezen?
De verwachtingen zijn hooggespannen: van hartschade tot diabetes, Parkinson, multiple sclerose, verlamming tot beroertes en kanker - de cellulaire allrounders hebben een bijna onuitputtelijk therapeutisch potentieel. Sommige behandelingspogingen zijn zelfs al succesvol geweest - maar alleen bij dieren. Zo konden verlamde ratten hun achterpoten weer bewegen na een stamcelinjectie. Wetenschappers vervingen het weefsel van muizen met hartaandoeningen die waren vernietigd door een hartaanval en genas de diabetes van diabetische knaagdieren. De resultaten klinken veelbelovend. Maar zolang ze niet bij mensen kunnen worden herhaald, zijn uitspraken over mogelijke therapieën nog ver weg.
Wat zijn de risico's van een eventuele stamceltherapie?
Wat stamcellen definieert en waarom ze worden beschouwd als hete kandidaten voor het herstellen van gebroken weefsel, is ook hun grootste risico: onbeperkte groei. Als stamcellen uit de hand lopen, kan dit leiden tot ongewenste weefselovergroei en in het ergste geval tot kwaadaardige tumoren. Hoe de controlemechanismen precies werken, is nog niet volledig opgehelderd. Maar dat is nodig om in het laboratorium stamcellen om te zetten in specifieke lichaamscellen.
De methoden van stamceltherapie zelf herbergen ook gevaren. Onderzoekers kunnen nu zonder de ethisch controversiële embryonale stamcellen. Maar het herprogrammeren van normale lichaamscellen tot geïnduceerde pluripotente stamcellen kan de genetische informatie beschadigen. Mutaties kunnen zich in de loop van het leven ook hebben opgehoopt in het genoom van lichaamscellen. Met de therapeutische cellen die daaruit worden gekweekt, worden deze genetische defecten echter ook in het lichaam van de patiënt gebracht. Ook dat kan leiden tot ongewenste groei en kanker.
Heeft het zin om voor uw kind stamcellen uit navelstrengbloed op te slaan?
Veel ouders denken dat ze door het bewaren van navelstrengbloed zorgen voor de genezing van hun kinderen in geval van ziekte. Leukemie (bloedkanker) wordt echter meestal behandeld met vreemd navelstrengbloed, omdat het navelstrengbloed zieke stamcellen bevat. Als de patiënt met deze cellen wordt behandeld, krijgt hij vroeg of laat opnieuw bloedkanker.
Veel particuliere aanbieders voor de opslag van navelstrengbloed adverteren dat verschillende ziekten zoals diabetes of multiple sclerose in de nabije toekomst kunnen worden genezen met behulp van stamceltherapie. Sterker nog, er is nog een lange weg te gaan en niemand kan precies zeggen wanneer stamceltherapie bij mensen mogelijk zal zijn. Ook het bewaren van navelstrengbloed is niet goedkoop. Een opslag voor 20 jaar kost ongeveer 2.000 euro. Daartegenover staan de openbare navelstrengbanken. Hier kunt u gratis navelstrengbloed doneren - en misschien het leven redden van een andere persoon met leukemie.
Tags: alcohol drugs sekspartnerschap alternatief medicijn